一款小分子药物的研发周期有多长?关键阶段有哪些?典型耗时与投入成本如何?
 2026西湖龙井茶官网DTC发售:茶农直供,政府溯源防伪到农户家
2026西湖龙井茶官网DTC发售:茶农直供,政府溯源防伪到农户家
研发一款小分子药物(即传统的化学合成药物,通常分子量较小)是一个漫长、高风险、高投入的过程。从靶点发现到最终获批上市,成功率极低(仅有约12%的进入临床阶段的分子最终获批),绝大多数项目失败。以下基于行业主流数据和可靠来源(如PhRMA、Tufts CSDD、FDA流程描述等)总结典型情况。
主要步骤(阶段) 小分子药物研发一般分为以下几个核心阶段:
1. 药物发现与铅优化(Discovery and Lead Optimization)
识别疾病相关生物靶点,进行高通量筛选化合物库,找到“击中”(hits),然后优化成“铅化合物”(leads)。涉及结构-活性关系(SAR)分析、药代动力学(ADME)优化等。这一阶段高度依赖计算化学、合成化学和生物筛选,通常耗时最长。
2. 临床前研究(Preclinical Testing)
在体外和动物模型中评估化合物的安全性、毒性、药代动力学和药效。完成IND(Investigational New Drug)申请所需数据,包括毒理学研究、动物药效等。
3. 临床试验(Clinical Trials)
- **I期**:小样本(20-100人)健康志愿者,主要评估安全性、耐受性和剂量。
- **II期**:中等样本(100-300人)患者,初步评估有效性和进一步安全性。
- **III期**:大规模(数百至数千人)随机对照试验,确认疗效、安全性和利益-风险比,为注册审批提供核心数据。
4. 监管审批(Regulatory Review)
向监管机构(如中国NMPA、美国FDA、欧盟EMA)提交NDA(New Drug Application)或类似申请,审查全套数据,包括CMC(化学、制造与控制)。审批通过后获批上市。
5. 上市后监测(Phase IV/Post-Marketing)
持续监测长期安全性、罕见不良反应、新适应症等。 这些阶段并非严格线性,常有迭代和失败。
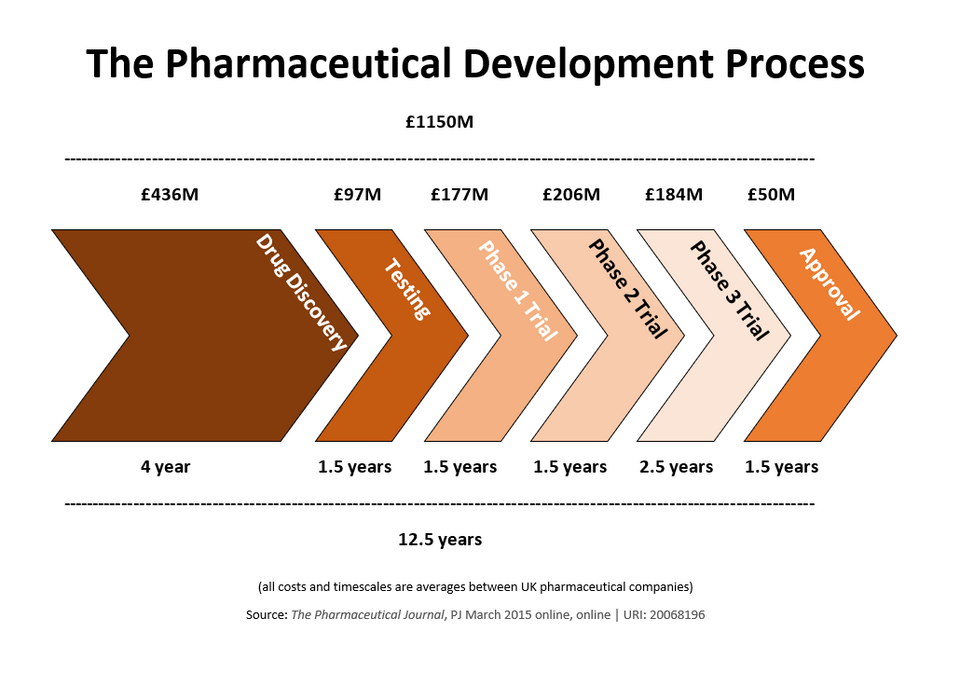
(上图为典型的药物研发流程图,展示了从发现到上市的阶段和成功率递减。)
周期(时间) 从靶点发现到最终获批上市,平均需要10-15年。
- 发现阶段:3-6年(有时更长)。
- 临床前:1-3年。
- 临床试验(I-III期):5-10年(III期最耗时)。
- 审批:0.5-2年。
实际周期因疾病领域、监管环境和技术难度而异。有些加速路径(如突破性疗法认定)可缩短,但整体仍很长。
研发费用(成本) 研发一款成功上市小分子药物的平均成本极高,主要因为需承担大量失败项目的开销(failure cost)和资金时间价值(capitalized cost)。
- 行业主流估计(如PhRMA、Tufts CSDD长期引用):**约26亿美元**(约合人民币180亿元左右),包括失败项目分摊和资本成本。这是2010s数据,但至今仍被广泛引用。
- 不同研究范围很大: 一些2024年分析显示,剔除部分因素后,出袋成本(out-of-pocket)平均约1-5亿美元,资本化后可达8-10亿美元左右,但包含失败后更高。
- 具体取决于治疗领域(如肿瘤、罕见病成本更高,抗感染较低)。
- 小分子药物相比生物制品(大分子、抗体药)通常成本较低(约25-40%便宜),合成路线相对可控、制造规模化更容易,但整体仍以数十亿美元计。 成本构成中,临床III期和失败项目占比最大。许多公司需同时推进多个项目以摊薄风险。
总结:小分子药物研发是高风险投资,成功一款往往需投入巨资和十余年时间。这也是为什么新药定价较高、仿制药和创新药并存的原因。实际项目中,时间和成本因具体靶点、疾病类型和公司经验而有很大差异。







































请先 登录后发表评论 ~